IEC 62304 軟體生命週期流程
IEC 62304 目前現行版本是 IEC 62304:2006/AMD 1:2015,用於確保醫療器材軟體的安全使用與維護,主要的應用在軟體本身就是醫療器材,或軟體內嵌或整合到醫療器材上的軟體。
IEC 62304 軟體生命週期流程
領導力企管與資策會聯合推出醫療器材軟體 - 軟體生命週期流程軟體( 試用申請已截止 )
什麼是 IEC 62304 醫療器材軟體-軟體生命週期流程
IEC 62304 目前現行版本是 IEC 62304:2006/AMD 1:2015,用於確保醫療器材軟體的安全使用與維護,主要的應用在軟體本身就是醫療器材,或軟體內嵌或整合到醫療器材上的軟體。
IEC 62304 應用範圍包含
- 韌體(firmware)和其他以軟體控制之醫療器材
- 單獨的軟體(stand-alone software)
- 安裝在一般用途電腦(general-purpose computers)上之軟體
- 專屬硬體/軟體醫療器材(dedicated hardware/software medical devices)
- 包含軟體或由軟體組成之醫療器材配件
※ 軟體交付予使用者之管道可由製造廠安裝(factory-installed)、第三方供應商安裝、現場安裝(field-installed)、網路平台下載安裝或升級(upgraded)。
醫療器材軟體的可能形式範例
A.醫療器材的附件
電子醫療器材本身內建的軟體,或為該器材的附屬物。
B.單獨的軟體
通常會和器材分開上市,可以處理、分析醫療儀器產生的資料,協助診斷、治療用途。
C.行動應用程式(Mobile Application『App』)
這類軟體可安裝在行動電話、平板電腦或其他電子產品 上,可能搭配醫療器材使用,此類應用程式若用於醫療目的, 則應符合醫療器材軟體之規定。
D.儲存軟體的記錄媒體(Record Media)
醫療器材軟體可以儲存於光碟、記憶卡(SD)、隨身碟等實體記錄媒體,或可經由網路伺服器線上下載。
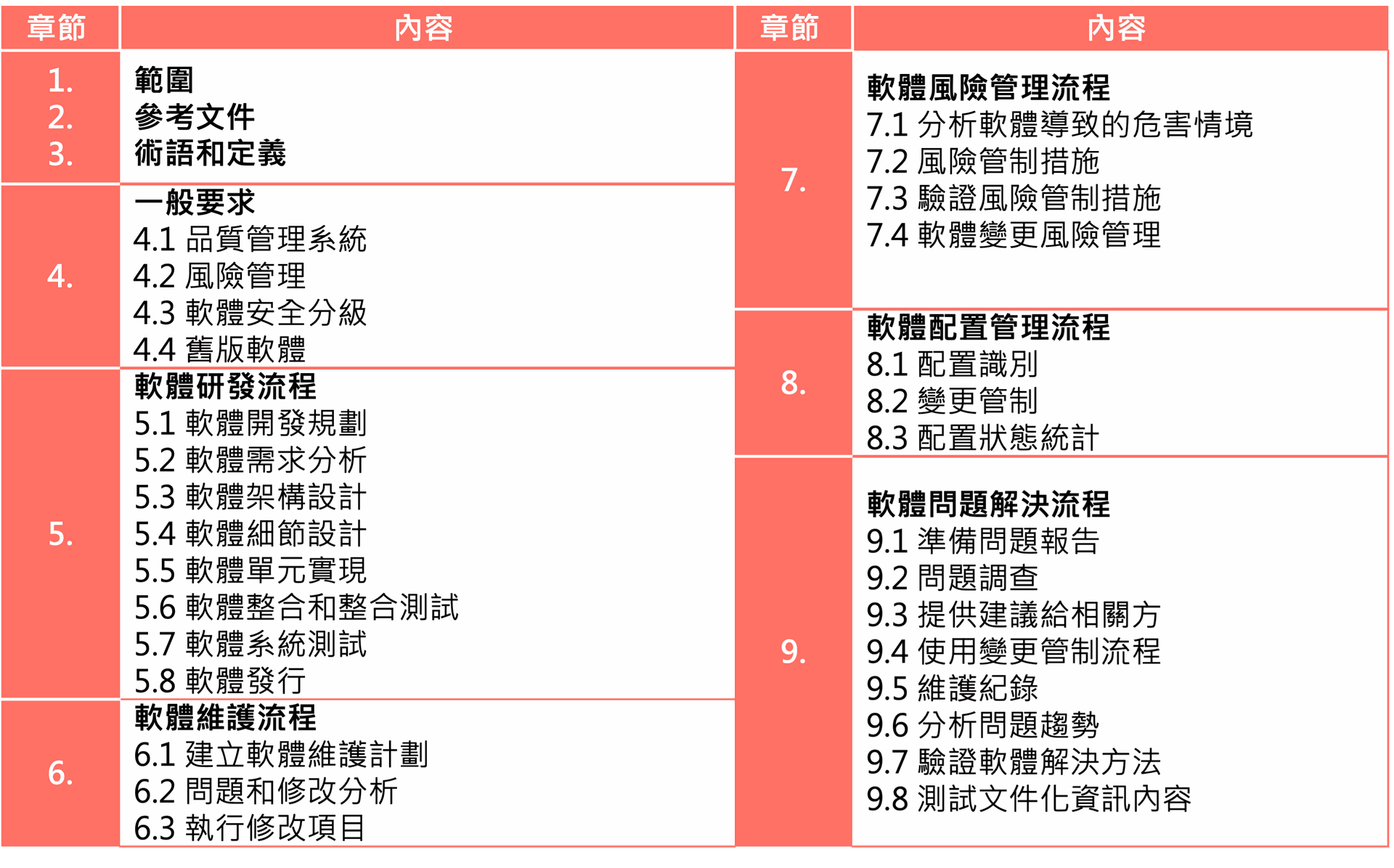
IEC 62304 的條文架構
IEC 62304 與其他標準的關聯性
在研發醫療器材時,會需要依據 IEC 62304 針對醫療器材軟體的研發與維護,這時為確保醫療器材的安全及有效性,IEC 62304 有必要與其它相關標準搭配使用。
1.ISO 13485 與 IEC 62304 的關聯性
ISO 13485 建構了醫療器材品質管理系統,確保有良好的品質管理環境可以研發各類產品,在使用的過程中,IEC 62304 與 ISO 13485 的關聯,主要落在設計開發的流程中,也就是說,在醫療器材軟體研發時,除了滿足 IEC 62304 的條文外,亦須滿足 ISO 13485 中與設計開發與識別追溯有關的條文。
【 ISO 13485 對照 IEC 62304 的相關聯條文 】:
| ISO 13485:2016 條文 |
對應 IEC 62304 條文 |
| 7.3.2 設計與開發規劃 |
5.1 軟體開發規劃 |
| 7.3.3 設計與開發輸入 | 5.2 軟體需求分析 |
| 7.3.4 設計與開發輸出 | 5.7 軟體系統測試 |
| 7.3.5 設計與開發審查 | 5.7 軟體系統測試 |
| 7.3.6 設計與開發驗證 | 5.8 軟體發行 6.3 執行修改項目 |
| 7.3.7 設計與開發確效 | 5.8 軟體發行 6.3 執行修改項目 |
| 7.3.9 設計與開發變更之管制 | 6.1 建立軟體維護計劃 |
| 7.5.8 識別 | 8.1 配置識別 |
| 7.5.9 追溯 | 8.2 變更管制 |
2.ISO 14971 與 IEC 62304 的關聯性
ISO 14971 已經妥善規劃醫療器材風險管理流程。IEC 62304 基於 ISO 14971 的規範,增加一些軟體需要的附加風險管理要求,特別是識別與軟體有關的風險因素,這些內容都在 IEC 62304 中進行歸納,作為軟體風險管理流程的一部分。
因此,執行 IEC 62304 的過程中,必須將 ISO 14971 的要求融合到醫療器材風險管理流程中。
【 ISO 14971 對照 IEC 62304 的相關聯條文 】 :
| ISO14971:2019條文 |
對應 IEC 62304 條文 |
| 5.4 鑑別危害和危害情境 |
4.3 軟體安全分級 7.1 分析軟體導致的危害情境 |
| 67.1 風險控制方案分析 | 7.2.1 定義風險管制措施 |
| 7.2 執行風險控制措施 | 7.2.2 軟體中執行風險控管措施 7.3.1 確認風險管制措施 |
| 7.5 風險控制措施引起的風險 | 7.3.2 記錄所有新的事件順序 |
| 8 風險管理審查 | 7.3.3 可追溯性紀錄 |
| 9 生產和生產後活動 | 7.4 軟體變更的風險管理 |
3.其他 可能與 IEC 62304 有關的標準
除了上述兩個最基本的標準外,其他比較常見可能與醫療器材軟體有關的標準還可能有 IEC 61010-1(醫療器材電氣設備)、ISO/ IEC/ IEEE 12207:2017(系統和軟體工程 - 軟體生命週期流程).. 等。
IEC 62304 完成後會產出什麼結果
IEC 62304 執行後的結果,有別於 ISO 13485 需要進行管理系統驗證,而是與 ISO 14971 的結果相同產出一份報告,醫療器材軟體製造商,會需要依據 IEC 62304 條文要求,完成一份專屬於產品的醫療器材軟體確效報告,依據軟體可能造成的危害情境,在風險管理流程中考量由軟體直接或間接引起的危害,將這些風險進行識別與管制。
如何完成一份符合 IEC 62304 規範的軟體確效報告
( 以下試用申請已截止 )
領導力企管與資訊工業策進會(資策會),共同合作開發了一套便於使用的軟體模組,只要醫療器材製造商根據軟體模組的指引及要求填入或上傳對應的資訊,即可快速又簡單地完成一份醫療器材軟體風險報告,總結來說使用領導力企管與資策會共台開發的模組可享有以下的好處:
1.確保條文要求沒有遺漏
軟體確效報告模組,依據條文的要求規劃,可確保使用者不會在不清楚條文的情況下發生遺漏。
2.滿足條文要求的結果
軟體確效報告模組,將條文的要求內化融入模組中,因此只要根據模組的指引,產出來的結果即可符合 IEC 62304 之要求。
3.查核重點說明
將複雜的條文簡化,直接列出重點,讓使用者可快速掌握條文要求。
4.範例說明
部分條文要求,提供清楚的範例,讓使用者在填寫過程中有明確方向。
5.資料填寫完成後可下載模板草稿
完成資料上傳即可獲得草稿,優化軟體確效報告專案管理能力。
6.資料填寫時遇到問題,領導力企管提供專業的顧問師群供客戶諮詢
軟體模組使用過程中遇到任何有關條文的問題,都會由領導力安排專任的顧問師協助您解決問題。

